+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Tetrahymena telomerase with CST | ||||||||||||
 マップデータ マップデータ | Tetrahymena telomerase with CST | ||||||||||||
 試料 試料 |
| ||||||||||||
 キーワード キーワード |  telomerase (テロメラーゼ) / RNP / CST / telomerase (テロメラーゼ) / RNP / CST /  REPLICATION (DNA複製) REPLICATION (DNA複製) | ||||||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報telomerase catalytic core complex assembly / telomerase RNA stabilization / telomerase RNA reverse transcriptase activity / DNA replication factor A complex / single-stranded telomeric DNA binding /  telomerase RNA binding / telomerase RNA binding /  telomerase holoenzyme complex / telomeric DNA binding / telomere maintenance via telomerase / telomerase holoenzyme complex / telomeric DNA binding / telomere maintenance via telomerase /  逆転写酵素 ...telomerase catalytic core complex assembly / telomerase RNA stabilization / telomerase RNA reverse transcriptase activity / DNA replication factor A complex / single-stranded telomeric DNA binding / 逆転写酵素 ...telomerase catalytic core complex assembly / telomerase RNA stabilization / telomerase RNA reverse transcriptase activity / DNA replication factor A complex / single-stranded telomeric DNA binding /  telomerase RNA binding / telomerase RNA binding /  telomerase holoenzyme complex / telomeric DNA binding / telomere maintenance via telomerase / telomerase holoenzyme complex / telomeric DNA binding / telomere maintenance via telomerase /  逆転写酵素 / DNA recombination / 逆転写酵素 / DNA recombination /  DNA複製 / DNA複製 /  chromosome, telomeric region / chromosome, telomeric region /  DNA修復 / DNA修復 /  DNA binding / zinc ion binding / DNA binding / zinc ion binding /  metal ion binding metal ion binding類似検索 - 分子機能 | ||||||||||||
| 生物種 |   Tetrahymena thermophila (真核生物) Tetrahymena thermophila (真核生物) | ||||||||||||
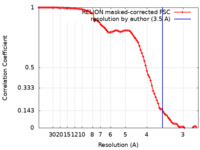
| 手法 |  単粒子再構成法 / 単粒子再構成法 /  クライオ電子顕微鏡法 / 解像度: 3.5 Å クライオ電子顕微鏡法 / 解像度: 3.5 Å | ||||||||||||
 データ登録者 データ登録者 | He Y / Song H / Chan H / Wang Y / Liu B / Susac L / Zhou ZH / Feigon J | ||||||||||||
| 資金援助 |  米国, 3件 米国, 3件
| ||||||||||||
 引用 引用 |  ジャーナル: Nature / 年: 2022 ジャーナル: Nature / 年: 2022タイトル: Structure of Tetrahymena telomerase-bound CST with polymerase α-primase. 著者: Yao He / He Song / Henry Chan / Baocheng Liu / Yaqiang Wang / Lukas Sušac / Z Hong Zhou / Juli Feigon /  要旨: Telomeres are the physical ends of linear chromosomes. They are composed of short repeating sequences (such as TTGGGG in the G-strand for Tetrahymena thermophila) of double-stranded DNA with a single- ...Telomeres are the physical ends of linear chromosomes. They are composed of short repeating sequences (such as TTGGGG in the G-strand for Tetrahymena thermophila) of double-stranded DNA with a single-strand 3' overhang of the G-strand and, in humans, the six shelterin proteins: TPP1, POT1, TRF1, TRF2, RAP1 and TIN2. TPP1 and POT1 associate with the 3' overhang, with POT1 binding the G-strand and TPP1 (in complex with TIN2) recruiting telomerase via interaction with telomerase reverse transcriptase (TERT). The telomere DNA ends are replicated and maintained by telomerase, for the G-strand, and subsequently DNA polymerase α-primase (PolαPrim), for the C-strand. PolαPrim activity is stimulated by the heterotrimeric complex CTC1-STN1-TEN1 (CST), but the structural basis of the recruitment of PolαPrim and CST to telomere ends remains unknown. Here we report cryo-electron microscopy (cryo-EM) structures of Tetrahymena CST in the context of the telomerase holoenzyme, in both the absence and the presence of PolαPrim, and of PolαPrim alone. Tetrahymena Ctc1 binds telomerase subunit p50, a TPP1 orthologue, on a flexible Ctc1 binding motif revealed by cryo-EM and NMR spectroscopy. The PolαPrim polymerase subunit POLA1 binds Ctc1 and Stn1, and its interface with Ctc1 forms an entry port for G-strand DNA to the POLA1 active site. We thus provide a snapshot of four key components that are required for telomeric DNA synthesis in a single active complex-telomerase-core ribonucleoprotein, p50, CST and PolαPrim-that provides insights into the recruitment of CST and PolαPrim and the handoff between G-strand and C-strand synthesis. | ||||||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_26863.map.gz emd_26863.map.gz | 5.3 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-26863-v30.xml emd-26863-v30.xml emd-26863.xml emd-26863.xml | 28.6 KB 28.6 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_26863_fsc.xml emd_26863_fsc.xml | 9.1 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_26863.png emd_26863.png | 98.2 KB | ||
| マスクデータ |  emd_26863_msk_1.map emd_26863_msk_1.map | 64 MB |  マスクマップ マスクマップ | |
| Filedesc metadata |  emd-26863.cif.gz emd-26863.cif.gz | 8.7 KB | ||
| その他 |  emd_26863_half_map_1.map.gz emd_26863_half_map_1.map.gz emd_26863_half_map_2.map.gz emd_26863_half_map_2.map.gz | 49.7 MB 49.7 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-26863 http://ftp.pdbj.org/pub/emdb/structures/EMD-26863 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-26863 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-26863 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_26863.map.gz / 形式: CCP4 / 大きさ: 64 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_26863.map.gz / 形式: CCP4 / 大きさ: 64 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Tetrahymena telomerase with CST | ||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.36 Å | ||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-マスク #1
| ファイル |  emd_26863_msk_1.map emd_26863_msk_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: half map 1
| ファイル | emd_26863_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | half map 1 | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: half map 2
| ファイル | emd_26863_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | half map 2 | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
+全体 : Tetrahymena telomerase holoenzyme
+超分子 #1: Tetrahymena telomerase holoenzyme
+分子 #1: Telomerase La-related protein p65
+分子 #2: Telomerase reverse transcriptase
+分子 #3: Telomerase holoenzyme Teb1 subunit
+分子 #4: Telomerase holoenzyme Teb2 subunit
+分子 #5: Telomerase holoenzyme Teb3 subunit
+分子 #6: Telomerase associated protein p50
+分子 #9: Telomerase-associated protein of 75 kDa
+分子 #10: Telomerase-associated protein of 19 kDa
+分子 #11: Telomerase-associated protein of 45 kDa
+分子 #7: Telomerase RNA
+分子 #8: Telomere DNA
+分子 #12: ZINC ION
-実験情報
-構造解析
| 手法 |  クライオ電子顕微鏡法 クライオ電子顕微鏡法 |
|---|---|
 解析 解析 |  単粒子再構成法 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 8 |
|---|---|
| 凍結 | 凍結剤: ETHANE |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD Bright-field microscopy / 最大 デフォーカス(公称値): 4.0 µm / 最小 デフォーカス(公称値): 0.8 µm Bright-field microscopy / 最大 デフォーカス(公称値): 4.0 µm / 最小 デフォーカス(公称値): 0.8 µm |
| 撮影 | フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 平均電子線量: 48.0 e/Å2 |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー















 Z
Z Y
Y X
X