+検索条件
-Structure paper
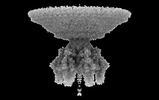
| タイトル | Molecular Architecture of Salmonella Typhimurium Virus P22 Genome Ejection Machinery. |
|---|---|
| ジャーナル・号・ページ | J Mol Biol, Vol. 435, Issue 24, Page 168365, Year 2023 |
| 掲載日 | 2023年12月15日 |
 著者 著者 | Stephano M Iglesias / Ravi K Lokareddy / Ruoyu Yang / Fenglin Li / Daniel P Yeggoni / Chun-Feng David Hou / Makayla N Leroux / Juliana R Cortines / Justin C Leavitt / Mary Bird / Sherwood R Casjens / Simon White / Carolyn M Teschke / Gino Cingolani /   |
| PubMed 要旨 | Bacteriophage P22 is a prototypical member of the Podoviridae superfamily. Since its discovery in 1952, P22 has become a paradigm for phage transduction and a model for icosahedral viral capsid ...Bacteriophage P22 is a prototypical member of the Podoviridae superfamily. Since its discovery in 1952, P22 has become a paradigm for phage transduction and a model for icosahedral viral capsid assembly. Here, we describe the complete architecture of the P22 tail apparatus (gp1, gp4, gp10, gp9, and gp26) and the potential location and organization of P22 ejection proteins (gp7, gp20, and gp16), determined using cryo-EM localized reconstruction, genetic knockouts, and biochemical analysis. We found that the tail apparatus exists in two equivalent conformations, rotated by ∼6° relative to the capsid. Portal protomers make unique contacts with coat subunits in both conformations, explaining the 12:5 symmetry mismatch. The tail assembles around the hexameric tail hub (gp10), which folds into an interrupted β-propeller characterized by an apical insertion domain. The tail hub connects proximally to the dodecameric portal protein and head-to-tail adapter (gp4), distally to the trimeric tail needle (gp26), and laterally to six trimeric tailspikes (gp9) that attach asymmetrically to gp10 insertion domain. Cryo-EM analysis of P22 mutants lacking the ejection proteins gp7 or gp20 and biochemical analysis of purified recombinant proteins suggest that gp7 and gp20 form a molecular complex associated with the tail apparatus via the portal protein barrel. We identified a putative signal transduction pathway from the tailspike to the tail needle, mediated by three flexible loops in the tail hub, that explains how lipopolysaccharide (LPS) is sufficient to trigger the ejection of the P22 DNA in vitro. |
 リンク リンク |  J Mol Biol / J Mol Biol /  PubMed:37952769 / PubMed:37952769 /  PubMed Central PubMed Central |
| 手法 | EM (単粒子) |
| 解像度 | 2.8 - 3.4 Å |
| 構造データ | EMDB-41649: P22 Mature Virion tail - C6 Localized Reconstruction EMDB-41651, PDB-8tvu: EMDB-41791, PDB-8u10: EMDB-41792, PDB-8u11: EMDB-41819, PDB-8u1o: |
| 由来 |
|
 キーワード キーワード |  VIRAL PROTEIN (ウイルスタンパク質) / VIRAL PROTEIN (ウイルスタンパク質) /  phage (ファージ) / phage (ファージ) /  bacteriophage (ファージ) / tail spike protein / TSP / gene product 9 (gp9) / Packaged DNA stabilization protein / gene product 10 (gp10) / bacteriophage (ファージ) / tail spike protein / TSP / gene product 9 (gp9) / Packaged DNA stabilization protein / gene product 10 (gp10) /  STRUCTURAL PROTEIN (タンパク質) / portal protein / head-to-tail protein / gene product 1 (gp1) / gene product 4 (gp4 / gene product 4 (gp4) / Tail hub protein / gene product (1) / Coat protein / Major capsid protein / gene product 5 (gp5) / Tailspike protein STRUCTURAL PROTEIN (タンパク質) / portal protein / head-to-tail protein / gene product 1 (gp1) / gene product 4 (gp4 / gene product 4 (gp4) / Tail hub protein / gene product (1) / Coat protein / Major capsid protein / gene product 5 (gp5) / Tailspike protein |
 ムービー
ムービー コントローラー
コントローラー 構造ビューア
構造ビューア 万見文献について
万見文献について